JUEVES 04 DICIEMBRE
Doctor (a):
Acceda a GinExeltis, la plataforma exclusiva de Exeltis Pharma México con contenido médico gratuito y de alto valor. Ayúdenos a validar sus datos para obtener acceso inmediato a recursos diseñados exclusivamente para profesionales de la salud.
No pierda la oportunidad de estar al día. ¡Complete su registro hoy!
Aviso de privacidadOsteoporosis: soporte nutricional integral para la salud ósea 16/01/2026 | 6 vistas
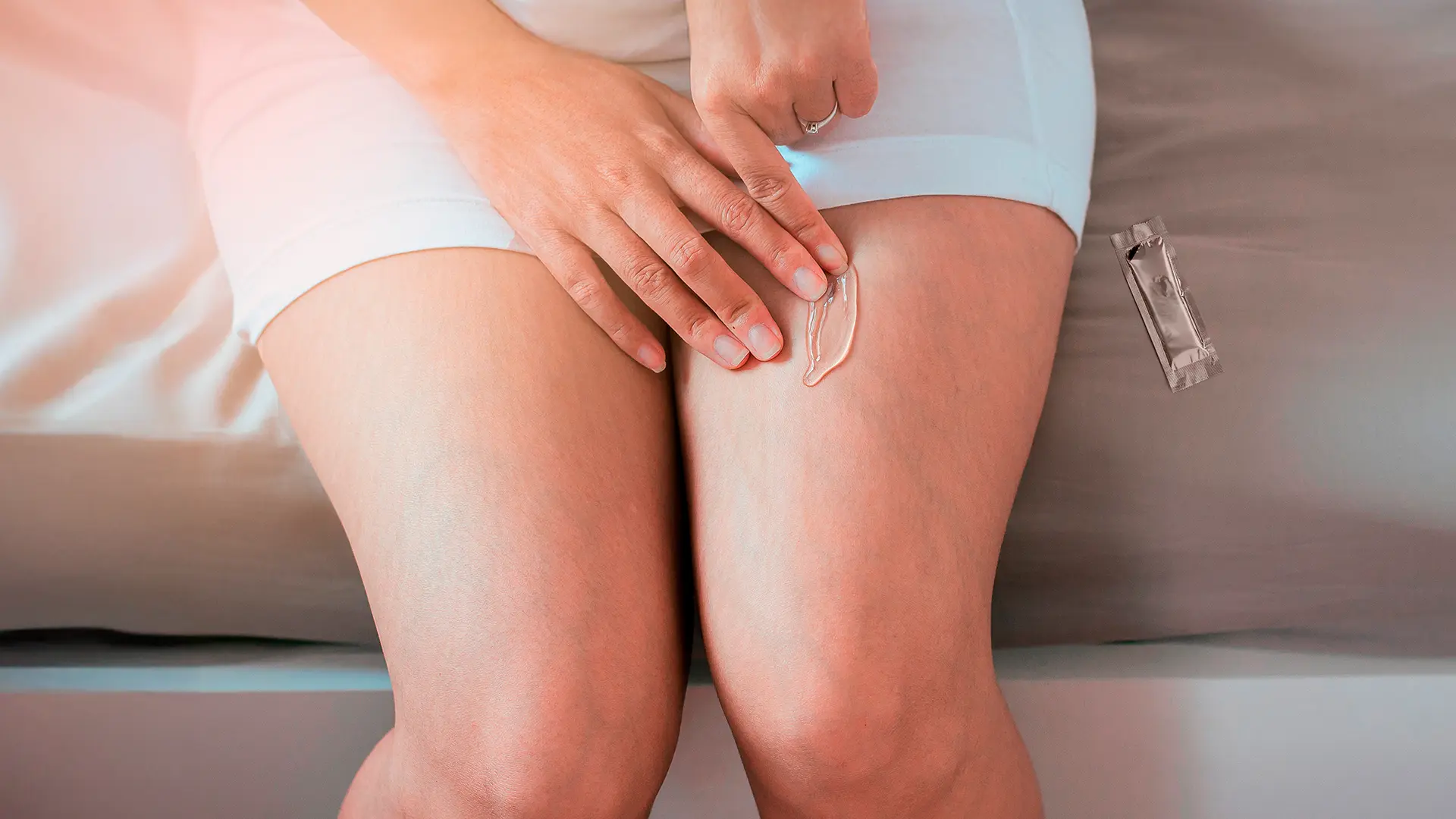
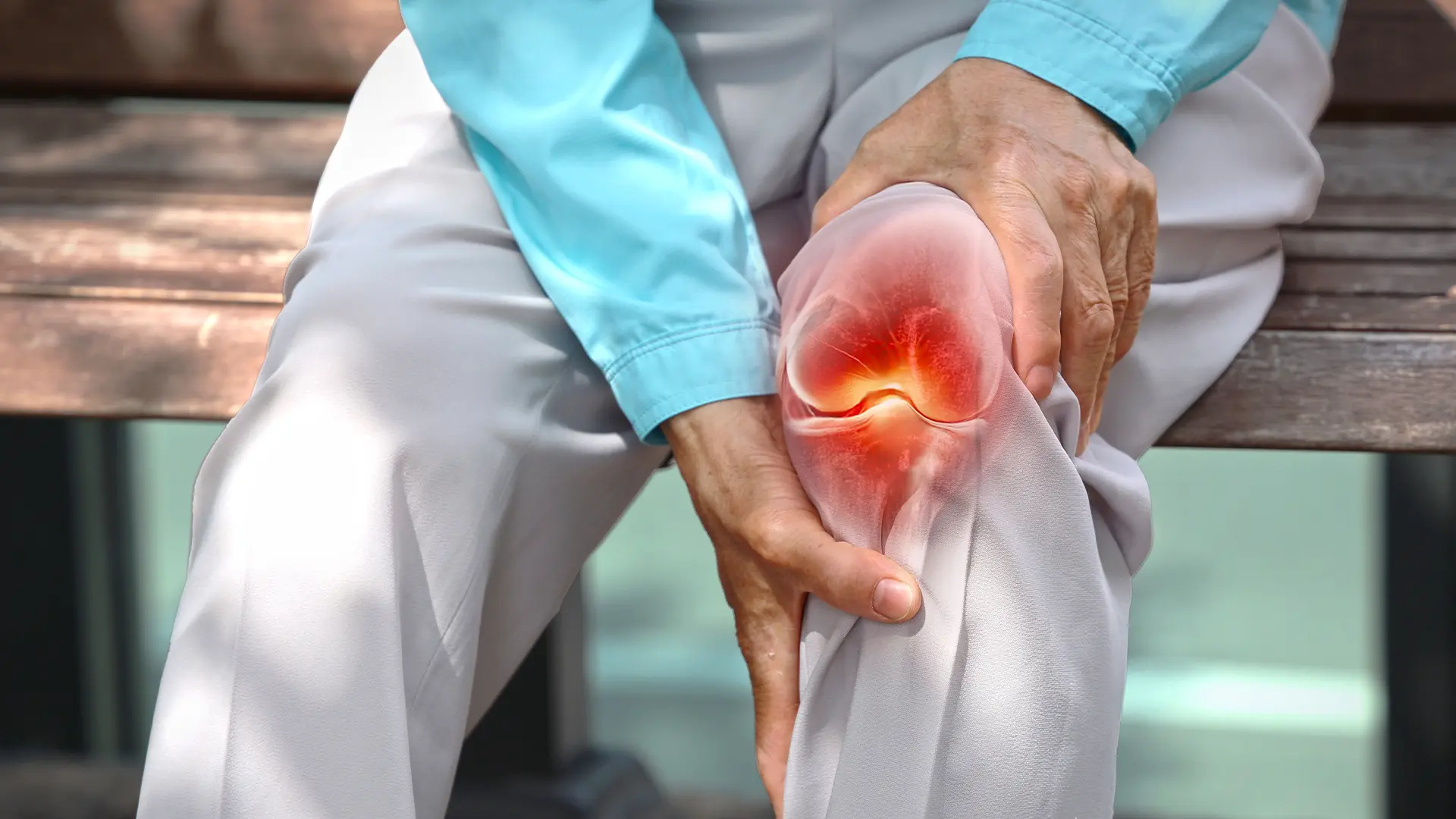
La osteoporosis es una enfermedad esquelética sistémica caracterizada por la disminución de la masa ósea y el deterioro de la microarquitectura del hueso, lo que incrementa de forma significativa el riesgo de fracturas. Su impacto es especialmente relevante en mujeres posmenopáusicas, etapa en la que la pérdida acelerada de masa ósea se asocia a cambios hormonales y a deficiencias nutricionales frecuentes. En este contexto, además del tratamiento farmacológico, el soporte nutricional adecuado representa un componente clave del abordaje integral de la salud ósea.Soporte nutricional óseo: una estrategia complementariaEl hueso es un tejido dinámico cuya resistencia depende tanto del contenido mineral como de la calidad de su matriz orgánica. Para su adecuado mantenimiento se requiere un aporte constante de nutrientes esenciales que actúan de forma sinérgica.El calcio es el principal componente mineral del hueso y su ingesta insuficiente se asocia con mayor pérdida ósea. La vitamina D es indispensable para la absorción intestinal del calcio y para mantener niveles séricos adecuados, siendo su deficiencia altamente prevalente en mujeres adultas y adultas mayores.La vitamina K2 participa en la activación de proteínas dependientes de vitamina K, como la osteocalcina, favoreciendo la correcta incorporación del calcio al tejido óseo y contribuyendo a la calidad ósea. Por su parte, el magnesio interviene en el metabolismo óseo, la síntesis de vitamina D activa y la función muscular, aspectos relevantes en la prevención de fragilidad y caídas.El colágeno, como principal proteína estructural del hueso, aporta soporte y elasticidad a la matriz ósea. Estudios clínicos han mostrado que su suplementación puede asociarse con cambios favorables en marcadores de remodelación ósea y densidad mineral en poblaciones específicas.En este sentido, Viplena, suplemento alimenticio que combina calcio, vitamina D, vitamina K2, magnesio y colágeno, ha sido formulado para brindar un soporte nutricional integral enfocado en la salud ósea, especialmente en mujeres posmenopáusicas y pacientes con riesgo de osteopenia u osteoporosis.ConclusiónEl manejo de la osteoporosis requiere un enfoque integral y sostenido que incluya tratamiento farmacológico cuando esté indicado, ejercicio, prevención de caídas y una nutrición adecuada. Los suplementos nutricionales formulados específicamente para la salud ósea, como Viplena, pueden desempeñar un papel coadyuvante, contribuyendo a cubrir déficits frecuentes de micronutrientes clave y apoyando la estructura y el metabolismo óseo. Su uso debe individualizarse y considerarse siempre como complemento —no sustituto— del tratamiento médico, dentro de una estrategia centrada en la prevención y el cuidado a largo plazo de la salud ósea.ReferenciasCompston JE, McClung MR, Leslie WD. Osteoporosis. Lancet. 2019 Jan 26;393(10169):364-376. Cosman F, de Beur SJ, LeBoff MS, Lewiecki EM, Tanner B, Randall S, Lindsay R; National Osteoporosis Foundation. Clinician's Guide to Prevention and Treatment of Osteoporosis. Osteoporos Int. 2014 Oct;25(10):2359-81. Knapen MH, Drummen NE, Smit E, Vermeer C, Theuwissen E. Three-year low-dose menaquinone-7 supplementation helps decrease bone loss in healthy postmenopausal women. Osteoporos Int. 2013 Sep;24(9):2499-507. Groenendijk I, van Delft M, Versloot P, van Loon LJC, de Groot LCPGM. Impact of magnesium on bone health in older adults: A systematic review and meta-analysis. Bone. 2022 Jan;154:116233. König D, Oesser S, Scharla S, Zdzieblik D, Gollhofer A. Specific Collagen Peptides Improve Bone Mineral Density and Bone Markers in Postmenopausal Women-A Randomized Controlled Study. Nutrients. 2018 Jan 16;10(1):97.
Síndrome de ovario poliquístico: más allá del ovario, el papel de la microbiota 16/01/2026 | 9 vistas
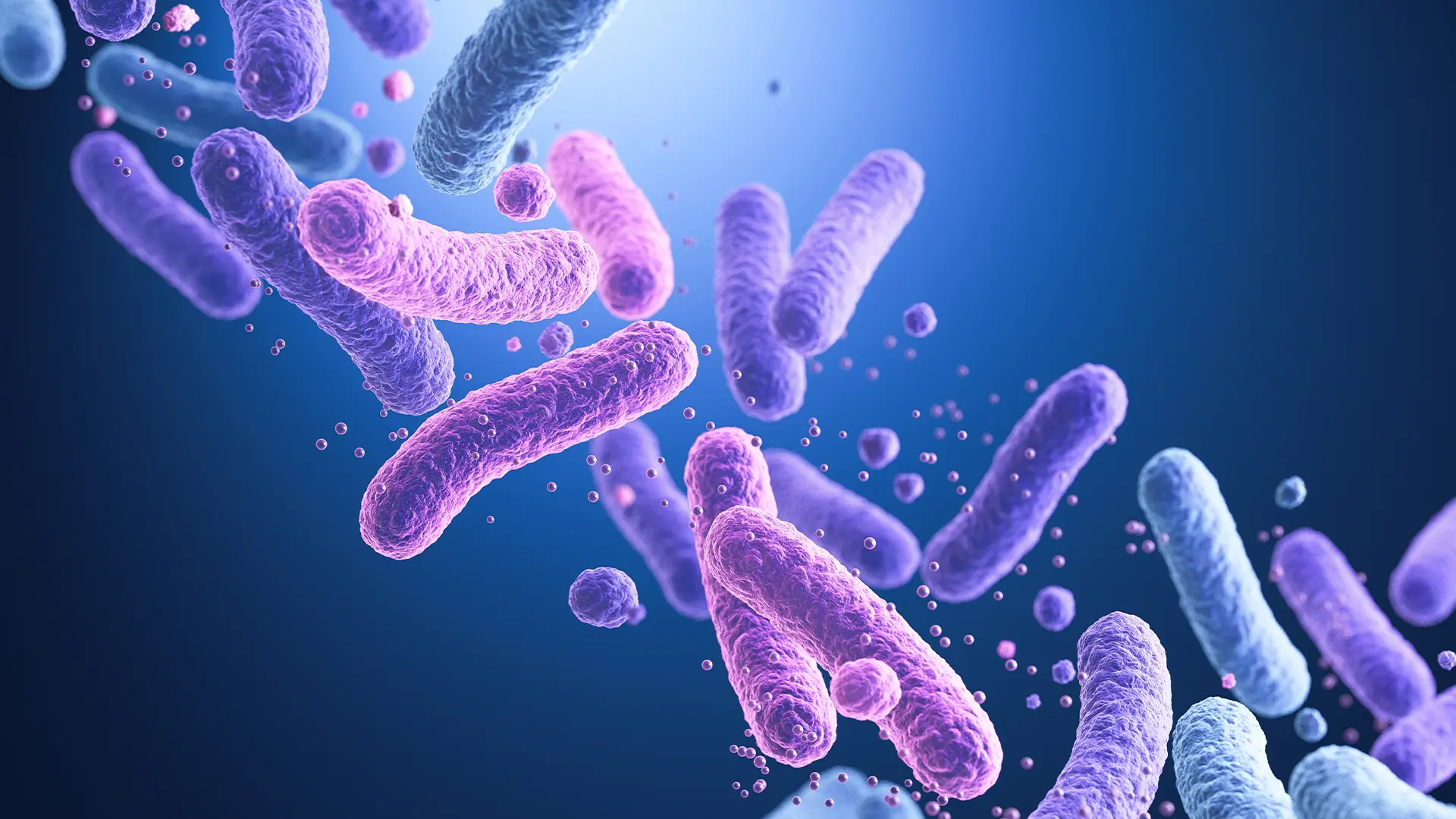
El síndrome de ovario poliquístico (SOP) es una entidad endocrino-metabólica compleja cuya fisiopatología va más allá del ovario. Evidencia emergente sugiere que la microbiota intestinal podría desempeñar un papel relevante en su desarrollo y expresión clínica.¿Cómo se relacionan el SOP y la microbiota?La Guía Internacional Basada en Evidencia 2023 establece que el diagnóstico de SOP en mujeres adultas requiere al menos dos de los siguientes criterios, una vez excluidas otras causas: hiperandrogenismo clínico o bioquímico, disfunción ovulatoria y morfología ovárica poliquística por ultrasonido o niveles elevados de hormona antimülleriana (AMH), reconociendo esta última como una alternativa diagnóstica válida.La microbiota intestinal (MI) participa activamente en la regulación del metabolismo energético, la inflamación de bajo grado y el equilibrio hormonal. Diversos estudios han demostrado que las mujeres con SOP presentan alteraciones en la diversidad y composición de la MI, con reducción de la α-diversidad y cambios en la β-diversidad, aunque con variabilidad entre poblaciones.A nivel composicional, se ha descrito un aumento de bacterias proinflamatorias como Bacteroidetes, Proteobacteria y Fusobacteria, junto con una disminución de géneros asociados a efectos metabólicos protectores. Estas alteraciones se han vinculado con resistencia a la insulina, disrupción del metabolismo de andrógenos e inflamación sistémica. Factores ambientales como dietas hipercalóricas, bajas en fibra, sedentarismo y obesidad influyen de forma significativa en la MI, mientras que patrones dietéticos como la dieta mediterránea y la actividad física regular parecen ejercer un efecto modulador favorable.Implicaciones clínicasDesde una perspectiva clínica, la modulación de la microbiota intestinal se perfila como un componente complementario dentro del manejo integral del SOP:Intervención dietética: Dietas ricas en fibra, con bajo índice glucémico y patrón mediterráneo se asocian con mejor perfil metabólico, reducción de inflamación y cambios favorables en la microbiota intestinal.Probióticos y prebióticos: Estudios preliminares sugieren que determinadas cepas pueden mejorar marcadores metabólicos e inflamatorios en mujeres con SOP, aunque la evidencia aún es heterogénea y no permite recomendaciones universales.Inositoles: Mio-inositol y D-chiro-inositol han mostrado beneficios en la sensibilidad a la insulina, la función ovulatoria y el equilibrio hormonal, y podrían ejercer parte de sus efectos a través de la interacción con la microbiota intestinal.Estas estrategias deben considerarse como adyuvantes, integradas a cambios de estilo de vida y tratamiento médico individualizado.ConclusiónLa evidencia disponible sugiere una interacción bidireccional entre SOP y microbiota intestinal, en la que las alteraciones metabólicas y hormonales pueden perpetuar la disbiosis, y viceversa. Aunque los datos actuales son prometedores, se requieren estudios prospectivos bien diseñados para definir el papel clínico de las intervenciones dirigidas a la microbiota como parte del abordaje integral del SOP.Referencias:Li J, Qiao J, Li Y, Qin G, Xu Y, Lao K, Wang Y, Fan Y, Tang P, Han L. Metabolic disorders in polycystic ovary syndrome: from gut microbiota biodiversity to clinical intervention. Front Endocrinol (Lausanne). 2025 Apr 28;16:1526468..Teede, H. J., Misso, M. L., Costello, M. F., et al. (2023). International evidence-based guideline for the assessment and management of polycystic ovary syndrome. Human Reproduction, 38(9), 1571–1643.
Rhodiola rosea: evidencia actual sobre su papel en estrés y fatiga 16/01/2026 | 6 vistas
El estrés crónico y la fatiga mental y física son motivos frecuentes de consulta en la práctica clínica actual. En este escenario, ha aumentado el interés por compuestos de origen natural con posible efecto modulador de la respuesta al estrés, entre ellos los denominados adaptógenos. Rhodiola rosea es uno de los más estudiados, aunque su papel clínico continúa en estudio.Evidencia disponible y mecanismos propuestosRhodiola rosea es una planta originaria de regiones frías de Europa y Asia, utilizada tradicionalmente para mejorar la resistencia física y mental. Sus principales compuestos bioactivos, las rosavinas y el salidrosido, se han asociado con la modulación del eje hipotálamo-hipófisis-adrenal, la regulación de cortisol y la influencia sobre neurotransmisores implicados en la respuesta al estrés, como serotonina y dopamina.Desde el punto de vista clínico, diversos ensayos controlados y revisiones sistemáticas sugieren que extractos estandarizados de Rhodiola rosea pueden reducir la fatiga relacionada con estrés y mejorar el rendimiento mental, particularmente en contextos de alta demanda cognitiva o emocional. Algunos estudios describen mejoras modestas en atención, concentración y percepción de agotamiento tras periodos cortos de suplementación.En el ámbito del rendimiento físico, los resultados son menos consistentes. Aunque se han reportado beneficios discretos en la percepción del esfuerzo y la resistencia, la magnitud del efecto es limitada y dependiente de la población estudiada y del diseño del ensayo.Implicaciones para la práctica clínicaEn la práctica clínica, Rhodiola rosea puede considerarse como un coadyuvante dentro de un abordaje integral del estrés y la fatiga, siempre con expectativas realistas y sin sustituir intervenciones médicas o psicológicas establecidas. Su perfil de seguridad es generalmente favorable, con efectos adversos leves y poco frecuentes; no obstante, se recomienda precaución en pacientes con trastornos del estado de ánimo o bajo tratamiento farmacológico concomitante.Aunque la evidencia sugiere un beneficio potencial modesto, se requieren ensayos clínicos de mayor calidad y mejor estandarización para definir con mayor precisión su papel terapéutico y sus indicaciones específicas.ReferenciasAmsterdam, J. D., & Panossian, A. G. (2016). Rhodiola rosea L. as a putative botanical antidepressant. Phytomedicine, 23(7), 770–783. European Food Safety Authority. (2012). Scientific opinion on the substantiation of health claims related to Rhodiola rosea. EFSA Journal, 10(8), 2805.Olsson, E. M. G., von Schéele, B., Panossian, A. G. (2009). A randomized, double-blind, placebo-controlled study of Rhodiola rosea in subjects with stress-related fatigue. Planta Medica, 75(2), 105–112. Panossian, A., & Wikman, G. (2010). Effects of adaptogens on the central nervous system and the molecular mechanisms associated with their stress-protective activity. Pharmaceuticals, 3(1), 188–224.Shafagh, R., et al. (2022). Effects of Rhodiola rosea supplementation on mental and physical fatigue: A systematic review. Nutrients, 14(10), 2042.
16/01/2026 | 6 vistas
10/12/2025 | 218 vistas
06/11/2025 | 380 vistas
06/11/2025 | 498 vistas
15/10/2025 | 458 vistas
Descubra Ginexeltis.mx: Su aliado en educación médica y ginecología
Ginexeltis.mx es la plataforma que conecta a médicos especialistas en ginecología con información confiable, herramientas prácticas y educación continua en salud femenina. Cada sección del sitio está diseñada para ofrecer un valor real a su práctica:
Todo al alcance de un clic: Desde la página principal, usted podrá acceder de manera rápida a los contenidos más relevantes: artículos, cápsulas educativas y próximos eventos. Su diseño intuitivo le permite encontrar la información que necesita en segundos, ahorrándole tiempo y esfuerzo.
Videos cortos y precisos sobre temas clínicos, tratamientos innovadores y guías médicas. Son ideales para médicos con agendas ocupadas que desean mantenerse actualizados sin perder tiempo.
2. Webinars y Eventos: Educación en vivo y bajo demandaParticipe en conferencias y talleres con expertos reconocidos, o consulte grabaciones de sesiones pasadas. Esta modalidad le permite acceder a conocimiento especializado y fortalecer sus habilidades clínicas desde cualquier lugar.
Artículos y estudios basados en evidencia que le ayudarán en la toma de decisiones clínicas. Contar con información validada le permite ofrecer a sus pacientes tratamientos actuales y diferenciados.
4. Noticias y Actualizaciones: Manténgase al díaReciba las últimas noticias de la industria, avances médicos y cambios en protocolos. Estar informado le permite anticiparse a cambios en su práctica y ofrecer siempre la mejor atención.
Con Ginexeltis.mx, la educación médica continua está al alcance de sus manos. Regístrese y descubra cómo mantener su práctica a la vanguardia de la ginecología y la salud femenina

 Casos Clínicos
Casos Clínicos
 Herramientas Digitales
Herramientas Digitales